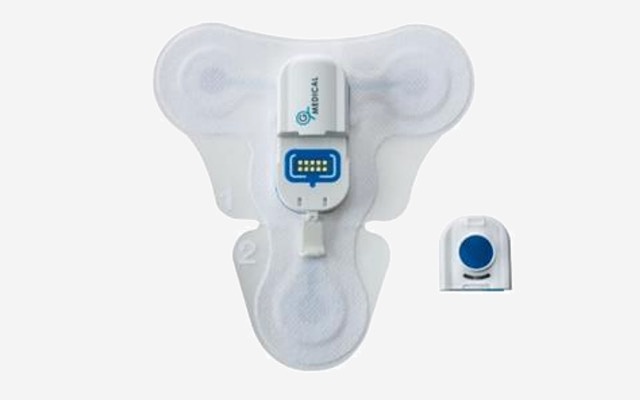
由医疗设备和远程医疗公司G Medical Innovations (ASX: GMV)开发的独立诊断检测设施(IDTF)平台已被美国四所大学医院采用,用于需要心脏和远程监测技术的患者。 每家医院的实施预计将导致患者数量的增加,同时在未来90天内,将逐步预订来自新注册患者的收入。 一旦患者被登记,他们将开始24小时至30天或更长时间的个性化监测服务,包括移动心脏遥测、动态心电监测和动态心电图。 这些医院已经处理了总共2000个病人的转诊。 新添加 G Medical首席执行官Yacov Geva博士表示,美国和其他国家的“大量医院”预计将被纳入该公司的IDTF目录。 他说:“到目前为止,IDTF主要是通过医生诊所、心脏病专家、电生理学家和内科医生提供的(但我们预计)医院部署将成为我们的主要收入来源,并为推广和销售我们的其他监测设备提供良好基础。” Geva博士补充说:“远程医疗是当前市场上一个不断增长的媒介,我们有信心将会逐步增加一些新医院,这将继续增加病人转诊。” 2019年,IDTF负责监测27,946名患者,根据目前的活动,预计到年底这一数字将增加三倍。 它的大部分收入来自较小的医疗设施,医院的实施被认为是扩大患者数量的关键催化剂。 IDTF平台今年的机构部署预计将超过G Medical 2019年IDTF收入542万美元(775万澳元)。 远程监控 G Medical自2014年8月成立以来,专注于开发下一代移动和电子健康解决方案及监测服务平台。 该公司专注于突破性技术,帮助提高医疗保健提供者的效率,并使患者能够更好地管理自己的健康。 G Medical的两个垂直产品——Prizma医疗智能手机壳和生命体征监测系统(VSMS)贴片——是专门为远程患者监测服务项目量身定制的诊断解决方案。 早盘中,G Medical的股价上涨8.93%,至0.061澳元。
Tag: GMV
G Medical的心脏监测贴片在美国授权用于冠状病毒紧急治疗
医疗设备和远程医疗公司G Medical Innovation Holdings (ASX: GMV)宣布获得美国食品和药物管理局批准,将其心脏监测贴剂用于正在接受冠状病毒治疗的患者的紧急情况。 今天早上公司摆脱暂停交易报告其生命体征监测系统(VSM)心电图(ECG)贴片收到紧急使用授权的远程监控一个心电图QT间隔的患者在医院接受冠状病毒治疗药物可以延长这些间隔并有可能引起致命的心律失常。 心电图上的QT间期显示了心室收缩和放松所需要的时间。QT间期延长意味着心脏肌肉在两次跳动之间需要更长的时间来充电。这可能是一个严重的发现,因为它表明有可能导致昏厥、癫痫或猝死的心律失常(心律失常)。 根据G Medical的说法,FDA的结论是,在这种情况下,由于全美医院心电监护仪的短缺,“没有足够的、批准的和可用的替代方案”来紧急使用VSMS贴片。 FDA还表示,远程监控可能会降低医护专业人员在大流行期间接触导致冠状病毒的病毒株的风险。 G Medical首席执行官Yacov Geva博士称赞该授权是“杰出的发展”,并表示“其价值不可低估”。 他说:“令人鼓舞的是,我们的技术被认为能够帮助减轻美国医疗系统的冠状病毒负担。” Geva医生补充说:“G Medical相信这种贴片可以填补美国医院所面临的心电图监测器短缺的问题,同时也能减少医护人员与疾病的接触。” VSMS patch G Medical的VSMS贴片被描述为“易于使用的临床级解决方案,用于在整个医疗生命周期中监视患者”。 使用可延长QT间期的药物治疗冠状病毒的成年患者可使用贴片长达14天。 在监测期间,贴片记录并传输心电图数据,数据保存后无线传输至G Medical诊断呼叫中心进行分析。呼叫中心的注册心电技师将汇编临床结果,并向医院的处方医生发送一份详细的报告。 供应链 G Medical目前在以色列的全资研发机构生产该贴片,并通过FDA和ISO认证的中东国家医疗设备合同制造商生产。 该公司计划未来在中国广州的一家工厂生产该贴片。 在今天的声明中,G Medical表示,它现在正在以色列工厂“积极”扩大该贴片的生产,预计很快就会有来自美国医院和医疗机构的需求。 目前,美国有超过150万的新冠肺炎确诊病例,预计未来几个月还会增加。 FDA的授权将继续有效,直到宣布情况存在证明终止授权的理由,G Medical声明。
G Medical获得了TGA的批准,设备可以用于对心脏病人进行持续监测
医疗设备和远程医疗公司G Medical Innovations (ASX: GMV)已经获得了治疗药品管理局(TGA)的批准,将设备用于病人入院前后心脏连续监测的心电图贴片GMP(G Medical Patch)扩展应用于该公司。 该公司表示,这一批准标志着一个重要的里程碑,因为作为IIa级医疗设备,该贴片现在正式符合所有相关的澳大利亚医疗和安全要求。 TGA认证是在2017年之前获得的欧洲CE II级批准的基础上增加的。 G Medical也在美国等其他目标市场寻求必要的监管批准。 G Medical首席执行官Yacov Geva博士说,TGA的批准证明了该公司的医疗设备和远程医疗技术与当前环境的关系。 他说:“我们的医疗设备和远程医疗平台被认为是成本效益高、可扩展的解决方案,可以减轻医疗系统的负担,病人和医生可以相对容易地采用和利用它们。” 他补充说:“我们的产品在当前的冠状病毒环境中是有效的和相关的,对于监测和远程管理慢性病患者以及与大流行同时发生和超出大流行的其他具体医疗适应症是重要的。” 临床级解决方案 G Medical的心电图贴片是模块化生命体征监测系统(VSMS)的一部分,是一种易于使用的临床级设备,用于整个医疗生命周期的患者管理。 它已被开发用于诊所、辅助生活住宅、医院和医疗服务提供者,并可以通过连续14天记录六通道心电图来简化和简化患者的治疗结果。 Geva医生说:“GMP旨在简化医疗生命周期所有阶段的病人管理,包括入院前、入院和出院后。” 他补充说:“这种产品可以提供更高水平的病人护理,减轻医务人员的负担,提高效率,减少责任,并(能够)减少再次入院的次数。” 上午10点左右,G Medical股价上涨17.02%,至0.11澳元。
HomeStay Care和G Medical准备通过电视提供下一代远程医疗服务
老年护理专家HomeStay care (ASX: HSC)和移动电子健康公司G Medical Innovations (ASX: GMV)公布了一项合作计划,这两家公司计划通过增强通信和远程监控能力,为患者提供下一代的护理服务。 在今天上午发布的一份市场声明中,两家公司宣布执行一项非独家分销协议,HomeStay将把G Medical的Prizma生命体征门户整合并分销到其技术平台,至少持续12个月。 集成的目的是为HomeStay的核心uVue远程健康平台和24小时监控响应中心提供远程生命体征监测功能,用于老年护理患者。 Prizma是一个完全被认可的远程生命体征监测系统,能够与智能设备一起执行个人生命体征测试。迄今为止,该设备已在美国、澳大利亚、新西兰、欧洲和台湾等多个司法管辖区获得批准。 该系统由一个移动医疗设备、一个智能设备应用程序和一个web门户组成,该门户可以将测试结果转发给位于不同位置的临床医生,也可以与现有的医生和护理团队进行远程共享。 填补老年护理的电子技术差距 HomeStay表示,老年护理是更广泛的医疗市场中一个高度专业化的细分市场,在确保老年患者和医生之间的充分沟通能力方面存在“重大挑战”。 这在很大程度上是因为大多数老年人缺乏技术意识,他们更喜欢简单的解决方案,比如电视,而不是相对复杂的工具,比如电子邮件、智能手机和电脑。 G Medical和HomeStay计划通过纠正现有的不足,并将现代技术的进步整合到现有的技术(如电视)中,来革新老年人护理支持。 uVue系统是一个基于云的远程医疗平台,当连接到电视时,提供一个简单的操作系统,只需要一个遥控器。 HomeStay表示,该服务提供四项关键功能,包括娱乐、信息、日历和远程健康功能。 据HomeStay称,其平台允许用户访问一系列娱乐选项,包括电视、视频、有声读物、向其他用户发送消息、访问显示重要约会和事件的自动日历,以及远程提供医疗管理、社交融入和医生咨询等健康服务。 G Medical的Prizma通过电视将整个服务推送给患者,它提供了一种简单易用的设备和接口,使患者能够远程无缝连接生命体征信息。 HomeStay董事总经理Graham Russell表示:“过去几个月,我们评估了几种解决方案,重点关注uVue远程医疗平台的无缝集成。” 他说:“我们觉得Prizma平台的可用性已经超出了我们的需求,我们期待着与G医疗团队合作。” 据G Medical称,Prizma平台将与uVue电视应用程序整合,通过屏幕信息提示居民每天记录自己的生命体征。该公司表示,这些结果将存储在云端,如果系统的分析检测到任何不良读数,那么该居民将“通过24小时的响应服务进行分类,以提供前瞻性的护理”。 此外,Prizma解决方案还通过向临床医生提供实时生命体征数据和关键信息,支持医生进行远程健康咨询。最终目标是改善潜在潜在问题的早期发现,从而促进老年护理患者的早期干预或预防护理。 G Medical首席执行官Yacov Geva博士说:“与HomeStay的这项协议是Prizma在改善日常消费者生活质量方面的适应性和潜力的另一个例子。” 他补充说,HomeStay的uVue平台是一个“独特的产品”,在G Medical计划在可预见的未来扩展到澳大利亚和新西兰之际,这对G Medical来说是一个重大机遇。 HomeStay承认,该协议尚未产生实质性的财务影响,并宣布,一旦整合完成,公司将“在可能的情况下”向市场更新设备使用情况。 这一消息推动G Medical股价上涨4.6%,至0.115澳元,HomeStay股价保持在0.006澳元不变。
G Medical获得Prizma智能手机健康监测器的美国非处方授权
移动和电子健康公司G Medical Innovations Holdings (ASX: GMV)的Prizma医疗智能手机已经获得美国食品和药物管理局(fda)的非处方授权。 该授权基于美国的COVID-19公共卫生应急政策,允许该设备在美国作为非处方产品销售,而不需要处方。 Prizma允许消费者将他们的智能手机变成一个移动医疗监测器来测量一系列的生命体征,包括温度、心率、压力水平和血氧饱和度,这些可以用来检测与感染和慢性疾病相关的症状。 用户可以将自己的医疗数据存储在云端,并与第三方(如医疗服务提供商和家庭成员)共享。 它被认为是目前市场上为医疗专业人员和患者提供全面的健康状况分析和监测的唯一解决方案。 美国食品和药物管理局承认,Prizma属于“测量或检测常见生理参数的非侵入性远程监测设备,用于在COVID-19突发公共卫生事件期间支持患者监测”的政策范围。 减少医疗负担 G Medical首席执行官Yacov Geva博士表示,获得非处方授权是该公司的一项重大成就。 他说:“这是一个巨大的进步,让我们可以直接接触到消费者、医生和医疗服务提供者,他们目前需要我们的解决方案。” “我们相信,该产品将受到欢迎,并有望帮助减轻(美国)医疗体系的负担。目前,美国医疗体系正面临与Covid19公共卫生紧急事件直接相关的能力挑战。” 他表示,G Medical目前正在制定战略,以打入美国消费市场,并利用这一“巨大的机遇”。 加快市场准入的商务谈判正在进行中。 该公司还将更新Prizma的包装,以反映美国食品和药物管理局的授权。