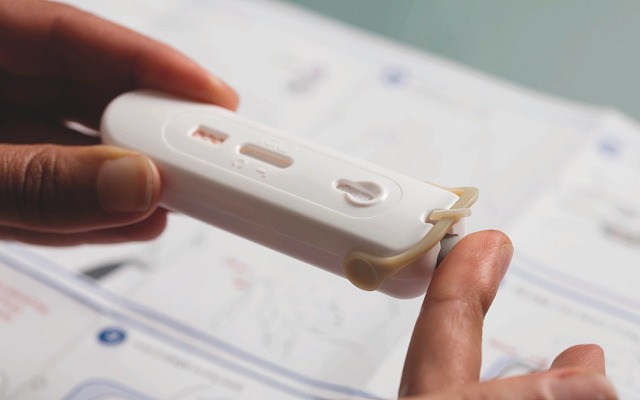
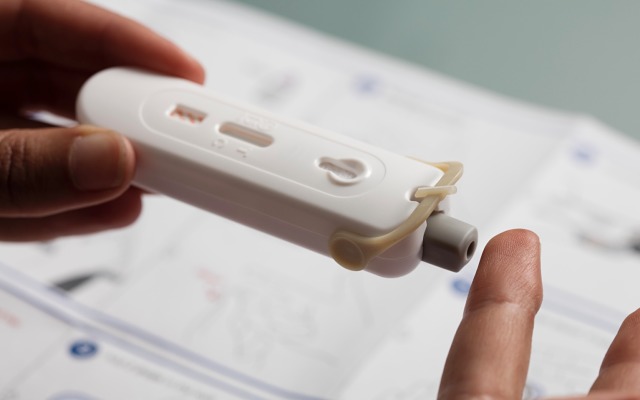
根据一项新的商业化协议,Atomo Diagnostics (ASX: AT1) 和 NG Biotech 将在澳大利亚、新西兰、加拿大和美国推出一种独特的基于血液的快速妊娠试验。 新的妊娠测试结合了 NG Biotech 制造的“高灵敏度 hCG 测试分析”和 Atomo 的集成 Pascal 血液测试设备。 众所周知,可检测到的 hCG 水平在血液中比在尿液中建立得更快——这使得这项新测试可能适用于早期妊娠诊断。 Atomo 预计其 Pascal 血液检测盒的“独特的易用性”和可靠性将为进入专业、场外交易和在线市场铺平道路。 协议条款 根据协议,Atomo 将向 NG Biotech 提供组装好的 Pascal 设备。 NG Biotech 还将获得使用这些设备制造快速妊娠测试的独家许可,这些设备将可用于家庭测试和专业用途。 初始协议为期五年,除非任何一方终止,否则将自动续订五年。 Atomo 将保留与其 Pascal 设备相关的所有 IP,而 NG Biotech 将保留与其 hCG 试纸相关的所有 IP 的所有者。 发行权 作为协议的一部分,Atomo 将拥有该产品在澳大利亚、新西兰、加拿大和美国的专业版和自测版的独家经销权。 Atomo 可以为 NG… Continue reading Atomo Diagnostics 和 NG Biotech 将基于血液的快速妊娠试验商业化
Tag: AT1
Atomo Diagnostics获得TGA批准,可向澳大利亚市场提供冠状病毒抗体检测试剂盒
医疗器械公司Atomo Diagnostics (ASX: AT1)的AtomoRapid (IgG/IgM)抗体检测试剂盒已获得治疗药品管理局的批准,该试剂盒用于疑似冠状病毒患者。 该测试能够确定病人是否产生了对该病毒的抗体,并能在15分钟内通过一滴血得到结果。 TGA的批准意味着该试剂盒将与Atomo HIV自我检测筛选试剂盒一起被添加到Atomo现有的澳大利亚治疗药物注册清单中。 然后将向澳大利亚实验室、医疗从业人员和居住和老年护理设施中的保健专业人员提供。 AtomoRapid与法国公司NG Biotech合作生产,NG制造测试条,Atomo制造设备并成为上市制造商。 TGA批准的检测试剂盒与NG目前在法国销售给消费者的试剂盒相同。 当地市场供应 Atomo联合创始人兼董事总经理John Kelly表示,TGA的批准将为当地市场提供一种高质量、可靠的快速抗体测试。 他说:“我们已经销售了澳大利亚唯一批准的艾滋病毒自检试剂盒,我们知道,我们的解决方案简化了在医疗现场的快速血液检测。” “让我们感到兴奋的是,我们的测试现在可以用于我们的国内(澳大利亚)市场,以协助抗击冠状病毒。” Kelly表示,该公司将考虑提交AtomoRapid接受墨尔本大学彼得•多尔蒂感染与免疫研究所(Peter Doherty Institute for Infection and Immunity)的评估。 维多利亚卫生部已委托该研究所协助新冠病毒快速检测的市场后验证工作,以告知其最佳用途。 独立研究 巴黎比塞特医院(Hopital Bicêtre)的一项独立研究利用Atomo的冠状病毒检测及其Pascal快速诊断检测平台,使用101名冠状病毒住院患者的血清检测IgM(早期感染反应)和IgG(持续感染反应)抗体。 试验发现,在出现症状15天后,敏感性和特异性分别为97.0%和100%。 另一项使用Atomo的Galileo平台进行的进一步研究检测了从确诊IgM和IgG阳性或阴性的患者中收集的78份阳性和22份阴性样本,发现症状出现15天后敏感性和特异性分别为96.8%和100%。 Kelly先生说,在Atomo的Pascal和Galileo装置上的研究结果表明,物质等效的结果都证明了100%的特异性。 商业机会 在获得TGA批准之前,Atomo就AtomoRapid在澳大利亚的商业分销渠道进行了初步讨论。 Kelly表示,该公司现在将涉足其认为冠状病毒抗体检测可以发挥重要作用的各个领域,包括公共卫生服务提供者、企业职业健康与安全以及老年人护理。 他说:“我们看到了我们的测试在许多渠道上的强大潜力,我们相信TGA的批准将加速这些机会。” “法国研究产生的性能数据和Atomo在该领域被证明的易用性,使我们的测试非常适合部署在一个大国,如澳大利亚的各种医疗点设置。” 他说,在澳大利亚的任何商业关系都将增加Atomo目前与Access Bio(覆盖美国和韩国市场)和NG Biotech(法国)离岸合作伙伴签订的冠状病毒测试收入增长供应协议。 根据现有合同,目前的大部分生产都是承诺的,初步分配给澳大利亚市场的10万单位,将根据需求扩大规模。
Atomo Diagnostics与美国生物技术公司合作,在全球销售新冠病毒快速检测包
新上市的医疗器械公司Atomo Diagnostics (ASX: AT1)与美国Access Bio公司签署了一项具有约束力的协议,该协议将允许Atomo的Galileo快速诊断测试(RDT)设备与Access的快速测试条一起用于新冠病毒抗体的检测。 Access目前提供了一种标准的新冠病毒快速血液检测,使用柳叶刀设备从患者皮肤生成血液样本,并使用单独的手动移液管收集血液并将血液输送到检测试纸上。 相比之下,这两个步骤——切割和收集——被集成到使用Atomo RDT设备的产品中。 Access和Atomo正在合作完成向美国食品和药物管理局提交新冠病毒综合检测试剂盒的紧急使用授权(EUA)所需的产品档案。 一旦获得相关的授权和批准,该试剂盒将由Access和Atomo联合品牌,在美国、加拿大和墨西哥上市。 Access将是上市制造商,并将保留向欧洲、澳大利亚、新西兰和东南亚以外地区销售产品的非独家权利,Atomo已与这些地区签订了合同。 协议条款 根据协议,Access必须在2021年9月之前销售至少200万辆RDTs和试车条,之后协议将以同样的义务和门槛延长12个月。 如果在2021年9月之前未能达到初始门槛,Access将向Atomo支付低于200万台的数量,其区域销售权将自动恢复为非排他性。 Atomo将从所有产品销售总收入中获得一定比例的收入,以考虑为Access提供Galileo盒式磁带。 及时的合作关系 Atomo董事总经理 John Kelly表示,两家公司的合作是及时的。 他说:“Access与美国市场有着紧密的联系,这是我们在新冠肺炎市场扩张的下一阶段的自然选择。” “基于血液的快速诊断检测是全球抗击新冠病毒的重要组成部分,鉴于美国的情况日益紧迫,我们很高兴能够在战胜这一大流行方面发挥自己的作用。” 容量升级 Kelly表示,Atomo正在提高生产能力,以满足协议规定的产量义务,并满足全球对其产品的需求。 产能升级的第一阶段将于本季度完成,总月设备产能将从每月约25万台增加到每月50万台。 该公司计划在今年年底前每月生产100多万台。 他表示:“未来12个月,我们仍将专注于提高产能,预计8月份将验证并实现首次增产。” “随着我们继续在艾滋病毒和新冠病毒市场推出我们的产品,这将支持全球对我们创新的快速检测解决方案日益增长的需求。” 今年4月,Atomo成为自2月底以来第一家在ASX上市的公司,也是第一家举办虚拟ASX上市仪式的公司。
Atomo Diagnostics确保了冠状病毒抗体测试的独家销售权
医疗器械公司Atomo Diagnostics (ASX: AT1)已经与现有的商业伙伴NG Biotech签署了一份补充协议,预计到今年年底将有超过200万份冠状病毒抗体测试销售。 这个消息紧随法国最近在巴黎比塞特Bicêtre医院进行的一项研究而来。研究人员对101例SARS-CoV-2感染住院患者的256份样本进行了检测,发现症状出现15天后,敏感性为97%,特异性为100%,阳性预测值为100%,阴性预测值为96.2%。 据Atomo介绍,该公司新开发的AtomoRapid 状病毒测试是一种综合血液测试设备,可确定患者是否产生了针对冠状病毒的抗体。 到目前为止,NG生物技术公司已经在法国订购了150多万台Galileo设备,用于其冠状病毒抗体测试。 检测结果可在15分钟内由一滴血产生,大大改进了现有的检测方法,这些方法需要实验室检测,并在得到阳性或阴性结果前几天转换。 市场排他性 Atomo表示,其Galileo快速检测设备作为艾滋病毒筛查快速检测在欧洲获得了专业和自检的批准。 这意味着,根据扩大后的协议,Atomo将获得在澳大利亚、新西兰和几个东南亚国家以AtomoRapid品牌销售和分销冠状病毒抗体测试的独家权利。 到目前为止,两家公司都没有与双方明确约定排他性期限,目前双方正在进行谈判,以达成最终的长期供应协议。根据补充协议,与NG生物技术公司的定价安排仅限于每单位应支付的价格,不包括任何许可费或专利费。 Atomo重要,获取独家权利在澳大利亚、新西兰和东南亚意味着它可以重新定位其市场提供作为上市状病毒制造商测试,从而成为唯一一家在澳大利亚TGA-approved类4自测,被列为“Atomo AIDS自测”澳大利亚注册的商品(ARTG)治疗。 Atomo在欧洲的分销已经获得了CE认证,因此它有信心与东南亚的监管机构取得联系,并已将香港、台湾和菲律宾列为其主要目标市场。 “在我们看来,这些结果以及Atomo设备在实地证明的易用性,使该测试非常适合社区部署和人口筛查项目。有了我们的独家协议和AtomoRapid COVID-19 (IgG/IgM)产品的CE认证,我们现在可以在未来几个月在我们的独家管辖范围内推进监管申请,”Atomo的联合创始人和常务董事John Kelly说。 在澳大利亚,尽管冠状病毒导致环境迅速变化,且不断发现与该疾病相关的新信息,Atomo仍在寻求验证其产品并证明其有效性。 在澳大利亚卫生部的协调下,Atomo打算邀请Peter Doherty感染和免疫研究所协助冠状病毒新型快速检测的上市后验证。 建立这一过程是为了更好地了解冠状病毒的工作原理,Atomo承诺在列入ARTG后提交其Galileo测试供Doherty研究所评估。 加强关系 今年4月,Atomo表示,它收到了NG生物技术公司的第二份采购订单,将提供另外55万套综合血液测试设备。NG生物技术公司在2020年3月签署了近40万台设备的初始订单,这使得NG公司可获得的设备总数达到947200台。 作为补充IPO招股说明书的一部分,Atomo宣布其计划在2020年总共销售250万台设备,两家公司承诺将为2020年后继续供应Atomo产品达成进一步的有约束力的购买协议。 根据协议条款,这家法国公司承诺订购与Atomo达成的月订单量的“至少70%”,但如果NG生物不能满足其最低订单承诺,Atomo有权取消交易。 Kelly说:“Atomo公司的快速检测设备提供可靠、用户友好的快速血液检测,作为全球应对冠状病毒大流行的一部分,我们正迅速采取行动应对。” 该公司还计划在欧盟以外销售其测试套件,以获得能够提高商业价值和可扩展性的大规模客户。一种方法是将重点放在医疗保健提供者和负责应对冠状病毒大流行的当局身上。 Focus目前正在完成NG生物技术公司下的前两个订单,该公司已经向法国国防部提供了测试。与此同时,我们仍在与两家总部位于美国的冠状病毒检测制造商就OEM检测设备的供应进行谈判。 该公司表示,将加快产能扩张,以满足对冠状病毒检测设备的持续需求,并继续支持现有的艾滋病经销商和其他OEM客户。 “Atomo很高兴获得独家市场,制造商列出,冠状病毒测试NG生物技术已成功发射与最初的销售在欧洲法国的军队(国防)和许多公立医院,在法国独立临床研究强劲业绩之后,”Kelly说。
Atomo Diagnostics在ASX上市前确保COVID-19测试设备的订单
在ASX上市前夕,生物技术公司Atomo Diagnostics (ASX: AT1)透露,它已经收到了用于COVID-19测试的专用快速血液测试设备的额外订单。 该公司今天宣布了来自法国诊断公司NG Biotech的第二份采购订单,将再提供55万台设备来测试针对COVID-19病毒产生的抗体,使设备订单总数达到947,200台。 这一消息是在周二,Atomo被接受为ASX官方名单之后传出的。预计该公司将于周四开始交易,市值为1.12亿美元(按每股0.20美元的首次公开发行(ipo)价格计算)。 这将使Atomo成为自2月27日以来首家在澳大利亚证交所上市的公司。此前,该公司通过IPO成功融资3,000万美元。 Atomo联合创始人兼董事总经理John Kelly在接受Small Caps采访时表示,Atomo是目前进入市场的“正确”公司。 他表示:“上市是一个艰难的市场,这一点毫无疑问,但我认为我们的业务正在增长,我们为COVID-19找到了一个非常好的解决方案。” 设备交付 Mr Kelly表示,NG Biotech 4周前收到的第一份订单已经发出,最新的订单涵盖5月至7月的供货。 快速诊断测试(RDT)设备被CE标记为全欧洲COVID-19测试的专业使用。 Mr Kelly表示,NG Biotech目前拥有在法国和英国销售的商业权利。 他表示,该公司正“非常迅速地”响应各方对其快速检测设备的兴趣,“提供可靠、用户友好的快速血液检测,作为全球应对COVID-19大流行的一部分”。 Mr Kelly表示:“目前的重点是完成NG生技公司下的前两笔订单,该公司已经在向法国国防部提供测试。” 根据目前的供应协议,NG Biotech有权在2020年购买最多246.5万台设备。 这两家公司有望在2020年后就Atomo产品的持续供应达成进一步的有约束力的采购协议。 Mr Kelly补充称:“与此同时,我们仍在与两家总部位于美国的COVID-19测试制造商进行谈判,以供应(原始设备制造商)测试设备。” 同样的技术也用于HIV检测 Atomo的快速检测平台最初是作为艾滋病毒筛查测试开发的,是澳大利亚唯一批准用于自检的艾滋病毒产品。 自2015年以来,该公司已经向医疗专业人员和消费者销售了超过55万个RDT,另外还向其他RDT制造商销售了43万个RDT用于分装。 Mr Kelly说:“我们已经有了唯一的HIV自检系统,它和COVID-19使用的是同一个快速检测平台,这就是为什么我们对它的可用性非常有信心。” Atomo的设备通过使用手指样本中的一小滴血,可以在15分钟内扭转结果。 “还有其他快速抗体测试,但其他公司已经商业化了一套‘盒子里的比特’化学仪器,所以做测试有点像12年级的科学实验;然而,Atomo实际上已经开发出了一种消费化的单一设备,它整合了所有这些步骤,并将其中许多步骤自动化,”Mr Kelly表示。 他补充说:“它让用户快速、轻松地进行测试变得更加可靠和简单。” 在今天的声明中,Atomo公司表示,将加快扩大生产能力的计划,以满足预期的COVID-19检测设备的持续需求,并继续支持公司现有的艾滋病毒分销商和其他制造客户。
Atomo Diagnostics首次公开募股3000万美元,目标是全球快速诊断测试市场
澳大利亚医疗设备制造商Atomo Diagnostics将首次公开发行(IPO)融资3,000万美元,以扩大其全球业务,并继续开发其专有的快速测试技术。 该公司本月早些时候与澳大利亚证券和投资委员会(Australian Securities and Investment Commission)联合推出了招股说明书,向澳大利亚和新西兰的机构投资者和散户投资者发行了1.5亿股新股,每股价格为0.2美元。 在上市之前,该公司已经接受了投资者2050万美元的投资承诺。 Atomo的快速诊断测试(RDT)设备被医疗专业人员和消费者用来筛查一系列疾病和医疗条件,包括艾滋病病毒感染。 自检是HIV诊断市场中一个相对较新的领域,世界卫生组织(WHO)于2016年批准了首个产品预审资格。 简化了流程 Atomo的技术声称可以简化基于血液的医疗诊断测试过程,并与更复杂和传统的基于血液的RDT试剂盒相比,减少错误。 艾滋病毒自我检测已在澳大利亚和欧洲获得监管批准,并已获得世界卫生组织(WHO)的资格预审,而其艾滋病毒专业使用检测也在澳大利亚和欧洲获得监管批准。 该公司董事长基思(John Keith)说,公司的技术消除了测试中的猜测。 “大多数当前的快速测试解决方案最初设计用于在实验室——这种类型的测试套件通常是复杂的,需要多个组件和无数每个测试步骤完成,并增加用户错误的可能性,这可能会导致不正确的诊断结果,减少了用户满意度水平,”他解释道。 “我们独特的集成设备旨在通过简化测试过程和减少用户步骤的数量来消除或减少现有测试套件格式中常见的错误。” 销售收入 自2015年实现商业化以来,Atomo已经通过非洲和欧洲的分销商,直接向澳大利亚市场销售了超过55万台专业用途和自用RDTs。 该公司还向其他快速诊断测试制造商出售了另外43万台RDTs,作为各种临床快速测试应用的子组件。 该公司通过与国际医疗公司Mylan Pharmaceuticals和Owen Mumford签订分销协议来销售产品,从而获得收入。 Atomo还将其RDT设备作为原始设备制造商产品提供给诊断测试开发人员,作为其最终测试产品的组成部分。 目前,根据与认证的第三方制造商的协议,Atomo外包子组装和测试设备的制造,以及组装和包装。 公司计划今年在南非的制造工厂开始组装Atomo艾滋病病毒产品。 全球扩张 基思表示,此次IPO将有助于Atomo扩大现有HIV检测工具的全球销售,并继续开发新的RDTs的其他临床应用。 他表示:“(我们的)大部分收入来自通过第三方分销商销售产品——这些安排使我们能够进入大型全球市场,而无需承担大量的销售和营销支出。” “这种方法为(我们)提供了一个有吸引力的平台,从这个平台可以增加现有产品的销售,同时专注于为新的临床应用开发快速测试产品。” Atomo在欧洲、非洲、南美、东南亚和澳大利亚的分销和销售都获得了必要的监管批准。 在获得了艾滋病毒检测工具的商业协议后,该公司表示,将把时间花在将更多的RDT产品商业化的机会上。 什么是RDTs? 快速诊断测试向患者使用者或医生提供快速结果,而不需要收集和将样本样本运送到实验室,也不需要处理与结果相关的数小时或数天的延迟。 RDTs通常在30分钟或更少的时间内提供结果,通常用作筛选测试或监测既存状况,使卫生保健专业人员能够在一次临床访问中进行测试和治疗。 这些检测被用于远离医院或集中实验室设施的分散环境中,包括在医院病房、诊所、药房、社区筛查项目和家庭中的实时检测。 它们通常不用于诊断或确认疾病,除非在一些缺乏广泛医疗基础设施的发展中市场。 RDTs在许多诊断应用中被发现,包括传染病的筛查、慢性健康状况的检测和监测,以及最近对消费者健康的促进。 艾滋病毒流行 联合国艾滋病规划署(UNAIDS)最近的研究显示,全世界估计有3790万人感染了艾滋病病毒。 该组织表示,2018年新增感染病例约170万,2017年死亡人数近80万,艾滋病仍然是一个重大的全球健康挑战。 2010年至2014年期间,122个低收入和中等收入国家的6亿多人接受了艾滋病毒检测服务,而仅在2017年,全球主要卫生捐助者就获得了1.22亿多例检测服务。 根据世界卫生组织和国际药品采购机制(UNITAID)的一份报告,2017年全球采购了1.83亿份艾滋病毒RDTs,不包括中国使用的1.5亿份RDTs。 报告指出,到2021年,对艾滋病毒RDTs的需求可能会增加到5亿次以上。 艾滋病毒自我检测最近成为一种可接受的、安全的和有效的方法,可用于接触高危人群,特别是那些可能不进行检测的人。 目前约有77个国家制定了支持艾滋病毒自我检测的政策,而其他许多国家正在制定此类政策。 基思表示,Atomo的艾滋病专业使用检测和未来利用Atomo设备进行的艾滋病快速检测,将进入一个与许多现有老牌公司竞争的市场。 Atomo Diagnostics的上市日期定在4月中旬。 该公司计划在ASX股票代码AT1下交易。